“深耕科技前沿动态,解读科技背后真相,瞄准科技产品评测”
在全球控制碳排放的背景下,合成生物学被视为未来实现可持续发展的必备工具,而绿色生物催化剂也正在成为各大跨国企业巨头争相研发和专利保护的关键材料。
“催化剂是化学合成过程中的一个关键环节。它不仅可以降低化学反应的活化能,加快化学反应的速率,还能增强反应的专一性,从而提升产品的纯度,减少废物排放,这对于工业生产来说是至关重要的。”华东理工大学(以下简称华理)生物化工教授许建和说。
其中,酶作为一种温和的绿色催化剂,赋予了生物催化可持续的属性,已成为可持续化工过程的重要一环。许建和教授及其团队长期专注于高活性、高选择性酶的开发,自主规划构建了一个数量达1200余种具有完全知识产权的工业先导酶库,例如,羰基还原酶及手性醇/胺脱氢酶等。
这些先导酶库中有限数量的“侦察兵”,能代表375万个羰基还原酶的基因序列,范围覆盖2000万个同类酶的结构及18亿条相似蛋白序列。从源头助力低成本高效率地生产高附加值功能化学品。
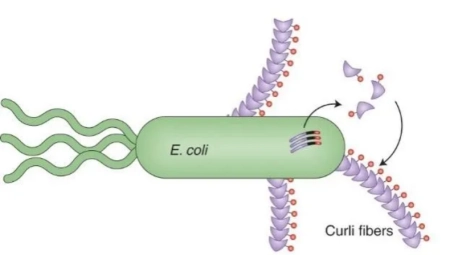
图基因修饰的大肠杆菌作为生产工程化菌毛生物膜的工厂(来源:Nature Chemical Biology)
诺奖指路绿色催化,酶催化剂成科研界“新宠”
一直以来,高性能催化剂的设计与合成都是化学领域的关键科学问题之一。诺贝尔化学奖也多次关注不对称催化领域。2018年,弗朗西斯阿诺德(Frances H. Arnold)由于进一步发展了酶的定向进化方法,大大加快了酶催化剂的设计速度,而获得了当年的诺贝尔化学奖;2021年,诺贝尔化学奖授予本杰明里斯特(Benjamin List)和大卫麦克米兰(David W.C. MacMillan),因其开发了模拟生物酶的有机小分子催化剂,并揭示了这种催化剂在不对称有机合成中的巨大应用潜力。
不难看出,“绿色”已成为诺奖考量的重要因素之一。在这种趋势下,化学反应的催化剂正向着安全、高效、低成本的方向发展,也因此激发了众多科学家们开发酶催化剂的热情。
事实上,酶被如此青睐原因有很多。首先酶是一种天然的生物催化剂,生物体内成千上万的化学反应均需各种功能不同的酶催化才能够发生并受到精准调控。更为重要的是,生物体内的合成过程自身就是可持续的,因此,酶催化的合成过程将有机会实现从原料到产品全周期的绿色生产。
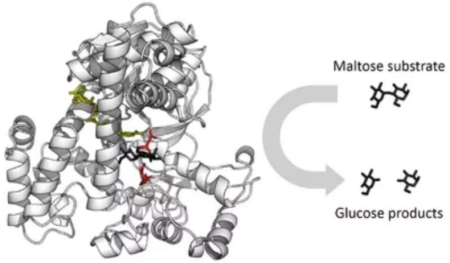
图葡萄糖苷酶将麦芽糖转化为两个葡萄糖示意图(来源:维基百科)
然而,酶也有一定的缺陷。许建和教授指出,酶是自然界的产物,它天生不是为工业生产服务的,而是为生物自己的生存和进化服务。天然的酶分子可能不太稳定或者活性很低,工业上应用的成本则会很高,导致产业化困难。
因此,掌握酶在工业应用上的难点和痛点,不仅是工业化应用的前提,且需要大量工程实践经验的积累。而提及绿色生物催化,就不得不提到许建和教授,长期以来,他一直致力于推动生物制造技术的实际落地和开花结果,并曾在生物反应器工程国家重点实验室工作长达二十多年,经验丰富,学术成果斐然。
探索产学结合之道,以“中试”加速规模化生产
生物化工的最终目标,就是将生物技术运用在生产过程中,并且大批量地制造目标产品。为了完成这一目标,许建和教授身体力行地践行产学相结合的理念,在工程应用领域中成果同样显著。其主持完成的代表性项目:生物催化剂的快速定制改造及高效合成手性化学品的关键技术,在与苏州富士莱医药股份有限公司的深度合作之下,成功地运用于(R)-硫辛酸的创新生产工艺之中,这在全球范围内属于开天辟地第一回。
硫辛酸具有与维生素类似的功能,其抗氧化性在医疗和保健上具有极高的价值,达维生素E 的500倍。合作企业通过绿色酶催化工艺合成的硫辛酸系列产品均获得世界卫生组织良好生产规范(Good Manufacturing Practice, GMP)的认证。
基于酶的构效关系解析和定向进化策略,该团队成功将天然羰基还原酶的催化效率提高960倍,稳定性提高1940倍,得到高性能的(R)-硫辛酸合成酶催化剂;在化学工艺上,该团队创新地采用“酶-化学偶联法”合成技术,相比于化学全合成工艺,使得产品合成步骤缩短一半,产品收率提高一倍以上,生产成本降低27%,三废排放减少45%。该项目见证了高效酶催化剂从实验室到工业应用的进化之旅。
不过,许建和教授也提醒道,“从实验室到生产线,优化和放大是亟需解决的关键工程问题。实验室的成果想要从试管放大到生产规模,蕴藏的风险非常大。因此,中试模拟是不可或缺的。”
实验室探索阶段,合成规模相对较小,显然无法和实际工业过程划上等号,且无法发现扩大化生产之后可能出现的问题。同时,大规模生产中的传质和传热过程需要进一步优化,而在实验室制备时并不需要考虑这些令科学家头疼的工程技术问题。
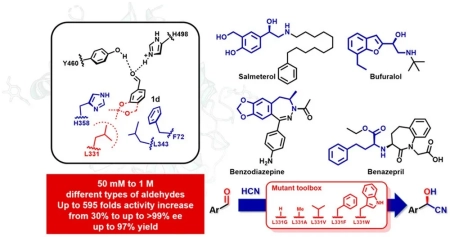
图团队近期工作,一种新的羟基腈裂解酶用于一系列非天然氰基氢化合物的合成[1](来源:ACS Catalysis)
基于此考虑,许建和团队从2003年起,就开始与江苏常州的一家企业合作进行中试。2012年,其团队在扬子江畔的常熟市国家开发区独立筹建生物合成中试工厂,付出诸多心血,最终搭建起完备的中试规模生产线,主要包括发酵制酶单元、催化反应单元、产品纯化单元等。其中,分离过程需要通过一系列的化工工艺,诸如萃取、离心、膜过滤、结晶和溶剂回收等单元操作实现反应产物的提取和纯化。“生物化工的内涵正体现于此,既包括了上游的生物制酶过程,又包括了催化反应和产品分离的化工过程,二者缺一不可。”许教授说道。目前,中试生产的产量大概在1 至10公斤,发酵罐体积300升,反应釜的容量处于10至 100升的范围。许建和认为,这样的条件完全可以模拟工厂的大规模生产工艺,从而找出其中存在的工程问题,然后进行系统优化,解决之后再放大,就可使产业化进程进一步加快。
未来生物催化潜力何在?或将是计算生物学与自动化实验室的融合
生物计算由于具有处理庞大数据和自我学习和进化的能力,已经成为许多学科的研究工具。许建和表示,他有理由相信生物计算将为酶在分子水平上的设计贡献独特的力量。
此前,谷歌旗下的 DeepMind 公司基于神经网络和深度学习,研发了能够用于生物医药领域的 AlphaFold2系统,可以用于从酶的一级序列预测三维结构,并针对酶的定向进化做一些引导性设计,从而缩小进化筛选的目标范围,大幅度减少实验工作量。
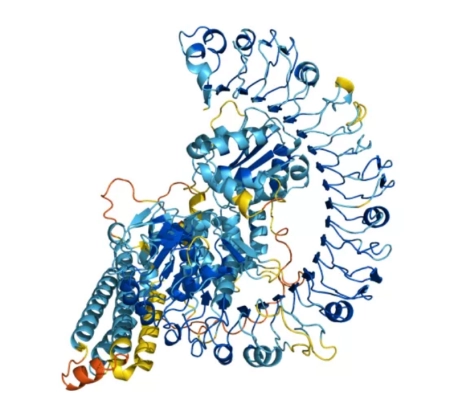
图一种潜在的植物抗病蛋白质的三维结构 Q8W3K0(来源:AlphaFold 官网)
现阶段,该程序只能从一级序列预测三维结构,但对于生物化学工程师来说,更关心的显然是三维结构与催化性能之间的关系。对此许建和表示,“在未来,我们要通过实验产生大数据,然后利用生物计算建立序列与功能的定量关系,这就是新一代生物催化技术的魅力和潜力所在。”
另一方面,自动化仪器和设备的引入将是必不可少的,它可以使数据通量呈指数级增长。同时,基础生物实验的成本,包括引物的合成、基因序列的测定等,将会下降一个数量级。如此一来,在同样的资金和人力成本的前提下,所产生的数据量将可能提高几个数量级,从而为计算生物学的应用提供大数据基础。
生物合成或将逐渐替代部分化学合成,想象无限,但路途遥远
据 Transparency Market Research 数据,2018年全球合成生物学市场空间已达到49.6亿美元,预计至2027年将超过400亿美元,市场空间巨大。与此同时,在化学品合成中,生物合成的比例会提高到一个新的阶段。而且,合成生物学的潜力远不止于此。
随着资本的投入、技术的累积、以及全行业自动化和人工智能技术的普及程度上升至临界点时,在未来,合成生物学将逐渐形成更加完整的产业链,生物制造的产品有望覆盖30%甚至一半左右化学产品(特别是各种天然产物和精细化学品)的制造,实现化工产业的生物化和可持续发展,这是大趋势。不过许建和教授也表示,对于生物制造而言,这既是机遇也是挑战。因为生物系统比化学系统更加复杂和难于预测,其研发周期更长且挑战性更强,我们也需要理性地看待。
参考:
1.Yu-Cong Zheng,Jian-He Xu. et al. ACS Catalysis,5757-5763(2020).
免责声明:内容来源于网络,版权归原作者所有。本文仅作信息交流之目的,文中观点不代表本号观点。如涉及版权问题,请及时联系我们删除。
想了解更多精彩内容,快来关注追求新知

